| МедСайт.ру |
Миокардиты
Что такое Миокардиты -Миокардит - поражение сердечной мышцы преимущественно воспалительного характера, обусловленное непосредственным или опосредованным через иммунные механизмы воздействием инфекции, паразитарной и протозойной инвазии, химических и физических факторов, а также поражение, возникающее при аллергических и аутоиммунных заболеваниях. Абсолютная частота миокардитов неизвестна, можно ориентироваться только на данные частоты встречаемости этого осложнения при различных заболеваниях. При дифтерии миокардит встречается у 20-30% пациентов, а летальность у больных дифтерией от кардиальных осложнений достигает 50-60%. У больных острыми респираторными вирусными заболеваниями миокардит диагностируется в 1-15% случаев. В период эпидемии гриппа клинические и инструментальные признаки миокардита обнаруживаются у 1-5% больных. ЕСНО-вирусы поражают миокард в среднем в 5% случаев, а энтеровирусы - в 5-15%. По данным ВОЗ в 1982-1996 гг., стабильное поражение сердечной мышцы при заражении вирусами Коксаки группы А развивалось в 3% случаев, при гриппе А - в 1,4% случаев, при гриппе В - в 1,2%, при парагриппе - в 1,7% и при аденовирусных инфекциях - в 1% случаев. При хронических инфекционных заболеваниях клинико-инструмен-тальные признаки воспалительного поражения сердца выявляются у 10-30% больных. При гепатите В миокардит отмечается у 5-15% больных, при клещевом Лайм-боррелиозе - у 15-20%, при токсоплазмозе - у 10-20%, при системном хламидиозе - у 5-20%. У ВИЧ-инфицированных поражение миокарда встречается в 20-40% случаев. В ряде случаев миокардит возникает вследствие перекрестных аутоиммунных реакций. Иммунный (аутоиммунный) миокардит может быть либо самостоятельным заболеванием, либо одним из синдромов при системных заболеваниях соединительной ткани или аллергических реакциях замедленного типа (реакция отторжения трансплантата, синдром Лайела, ожоговая болезнь). При ревматоидном артрите поражение сердца выявляется у 5-25% больных, при системной склеродермии - у 20-40%, при системной красной волчанке - у 5-15% пациентов. При ожоговой болезни признаки миокардита выявляются в 20-40% случаев. Миокардит может быть вызван воздействием на сердечную мышцу токсических веществ или физических факторов (например кардиотоксин - при дифтерии, ионизирующее излучение - при лучевой терапии опухолей средостеия). По данным патологианатомических исследований, признаки воспалительния миокарда обнаруживают в 4-9% аутопсий. Средний возраст заболевших составляет 30-40 лет. Женщины заболевают миокардитом несколько чаще мужчин, но у мужчин чаще встречаются тяжелые формы заболевания. Несмотря на то что миокардит был выделен в качестве самостоятельного заболеванря более 200 лет назад, до сих не решены вопросы этиологии, патогенеза, клинической диагностики и специфического лечения этого заболевания.
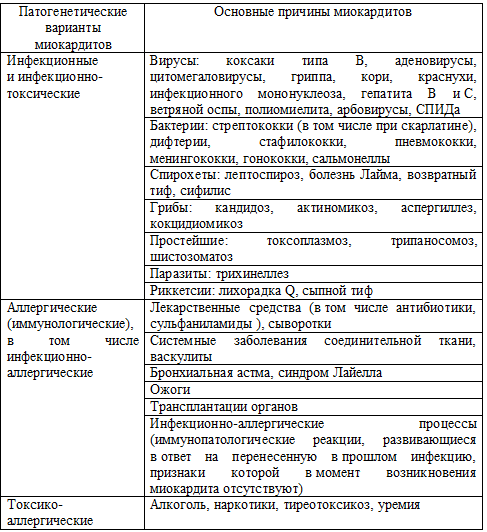
Что провоцирует / Причины МиокардитПричины миокардитов весьма разнообразны (таблица 26). Наиболее частыми из них являются инфекции (вирусные, бактериальные, риккетсиозные, спирохетозные, паразитарные, грибковые), которые служат причиной так называемых инфекционных или инфекционно-токсических миокардитов. Вызвать миокардит может практически любой инфекционный агент, однако более чем в половине случаев возбудителями миокардитов являются вирусы, в первую очередь, энтеровирусы Коксаки типа В. Важную роль в возникновении инфекционных миокардитов отводят также цитомегаловирусам, аденовирусам, вирусам гриппа, кори, краснухи, инфекционного мононуклеоза. Наиболее известными из бактериальных инфекционно-токсических миокардитов являются дифтерийный и скарлатинозный миокардиты. Дифтерийный миокардит осложняет течение этого инфекционного заболевания в 10-25% и отличается очень тяжелым прогнозом (летальность - 50-60%). Вторая группа причин, вызывающих аллергические (иммунопатологические) миокардиты, объединяет различные заболевания и синдромы, в основе которых лежат аллергические или иммунопатологические реакции, в том числе на применение лекарственных препаратов, сывороток. Нередко аллергические (аутоиммунные) миокардиты развиваются при системных заболеваниях соединительной ткани, бронхиальной астме, синдроме Лайелла, ожогах, трансплантациях сердца. К этой же группе причин миокардитов относятся иммунопатологические (аутоиммунные) процессы, которые развиваются в результате перенесенной в прошлом инфекции, вирусной инфекции Коксаки типа В. Как правило, на этой стадии заболевания присутствия вирусных частиц в кардиомиоцитах и интерстициальной ткани обнаружить не удается. Отсутствуют также внесердечные проявления инфекции. В этих случаях основное значение в возникновении воспаления сердечной мышцы имеет клеточный и гуморальный иммунный ответ, “запущенный” инфекционным агентом, при котором миокард инфильтрируется Т-лимфоцитами, IgG, аутоиммунными антителами, комплементом и другими агрессивными иммунными факторами, повреждающими кардиомиоциты. В этих случаях речь может идти об инфекционно-аллергических миокардитах, которые нередко представляют собой лишь дальнейшую стадию повреждения сердечной мышцы инфекционным агентом.
Таблица 26. Основные причины миокардитов К третьей группе причин миокардитов относятся заболевания и патологические состояния, для которых типично прямое токсическое воздействие на миокард различных химических и биологически активных веществ (тиреотоксикоз, уремия, алкоголь), вызывающее иммунное воспаление сердечной мышцы с признаками реакции гиперчувствительности замедленного типа. Миокардиты, обусловленные этими причинами, принято называть токсико-аллергическими миокардитами.
ЭТИОЛОГИЧЕСКИЕ ВАРИАНТЫ МИОКАРДИТОВВирусный миокардит Вирус Коксаки В является РНК-содержащим вирусом - одним из представителей группы энтеровирусов. Вирусный (Коксаки В) миокардит является наиболее частой этиологической формой миокардитов, и это должно обязательно учитываться при диагностике. Кроме того, вирус Коксаки В является также ведущей причиной острых миоперикардитов. Для вируса Коксаки В типична высокая кардиотропность. Современные методы исследования позволяют обнаружить его в кардиомиоцитах, в перикарде, в клапанах сердца. Вирус Коксаки В может вызвать развитие миокардита в любом возрасте, хотя, как указывалось ранее, чаще болеют лица среднего и молодого возраста. Миокардит, вызванный вирусом Коксаки, часто развивается у лиц в возрасте старше 50 лет. Этот миокардит может развиться и у людей, страдающих ишемической болезнью сердца, что, конечно, затрудняет диагностику. Около 60% страдающих Коксаки-миокардитом и миоперикардитом составляют мужчины. У женщин заболеваемость Коксаки-миокардитом чаще наблюдается во время беременности и в послеродовом периоде. При поражении вирусом Коксаки во время беременности миокардит может развиваться у плода и быть причиной мертворождения. В силу указанных причин возможно развитие миокардита у новорожденных, а также в первые 6 месяцев жизни. Для Коксаки-миокардита характерна сезонность. Заболевание чаще развивается летом и осенью, по данным Karjalainen (1984), наиболее высокая заболеваемость отмечается в мае, ноябре, декабре. Клиническая картина вирусного (Коксаки В) миокардита в целом соответствует описанию симптоматики миокардита, сделанному нами ранее. Следует только отметить, что перед развитием кардиальной симптоматики у большинства больных отмечается лихорадка и синдром гастроэнтерита (неинтенсивные боли в эпигастрии, возле пупка, тошнота, рвота, нечастый, обильный водянистый стул без патологических примесей). В клинической картине Коксаки В миокардита наряду с симптомами миокардита часто присутствуют плевродиния (боль, обусловленная вовлечением в патологический процесс плевры, усиливающаяся при дыхании и кашле), лимфаде-нопатия, спленомегалия, орхит. Установлены особенности течения Коксаки-миокардита в зависимости от возраста. У молодых людей в возрасте 16-20 лет миокардит протекает с выраженной клинической симптоматикой, часто с присоединением перикардита или плеврита, течение миокардита острое, как правило, заканчивается выздоровлением. У лиц в возрасте старше 40 лет симптоматика миокардита развертывается более постепенно, отчетливо доминирует выраженная кардиалгия, которая может сохраняться длительное время (заболевание часто принимается за ИБС). Могут наблюдаться одышка и сердцебиения. При диагностике вирусной (Коксаки В) этиологии миокардита необходимо учитывать: наличие симптоматики острого гастроэнтерита в периоде, предшествующем развитию клиники миокардита, не менее, чем четырехкратное нарастание титров специфических вируснейтрализующих антител в парных сыворотках кровибольного, обнаружение вируса или вирусного антигена в фекалиях больного с помощью электронной микроскопии, иммуноэлектроос-мофореза, выделение вируса в культуре клеток из различных биологических субстратов (смывы из зева, фекалии), определение РНК вируса Коксаки в крови больного и в био-птатах миокарда методом полимеразной цепной реакции. У большинства больных Коксаки В миокардит протекает благоприятно, больные выздоравливают в течение нескольких недель, однако иногда наблюдается развитие дилатационной кардиомиопатии, возможны летальные исходы. Септический миокардит Септический миокардит - это бактериальный миокардит, развивающийся при сепсисе и характеризующийся внедрением инфекционного агента в миокард. На долю септического миокардита в современных условиях, при лечении сепсиса высокоактивными антибиотиками, приходится около 1,5-4% всех миокардитов. Основными возбудителями септического миокардита являются стафилококки, синегнойная палочка, кишечная палочка, сочетание этих видов флоры. Патоморфологическая картина септического миокардита достаточно характерна. При макроскопическом исследовании сердце увеличено в размерах, имеет «дряблый», «вареный» вид, в толще миокарда могут быть очаги кровоизлияний. При микроскопическом исследовании обнаруживаются значительный интерстициаль-ный отек миокарда, тромбоцитарные и эритроцитарные микроагрегаты в микроциркуляторном русле, а также множественные клеточные инфильтраты в миокарде, состоящие из нейтрофилов, гистиоцитов, лимфоцитов (в инфильтратах четкое преобладание нейтрофилов). В кардиомиоцитах определяется дистрофия (белковая, вакуольная), миолиз, расщепление миофибрилл (возможен диско-идный распад). Характерно также обнаружение в миокарде микроорганизмов. Особенно большие участки миолиза кардиомиоцитов наблюдаются при синегнойном сепсисе. Септический миокардит всегда протекает с выраженной клинической картиной, обычно речь идет о тяжелой форме миокардита, и он может быть непосредственной причиной смерти больных сепсисом. Симптоматика септического миокардита соответствует вышеописанным проявлениям. Однако, по мнению профессора Палеева Н.Р. для септического миокардита в отличие от вирусного характерна выраженная тахикардия, при этом наблюдается несоответствие между частотой сердечных сокращений и температурой тела, могут отмечаться мерцательная аритмия и пароксизмальная тахикардия. Выраженная тахикардия при септическом миокардите объясняется активацией симпатического отдела вегетативной нервной системы, системы цитокинов, стимуляцией синтеза провоспалительных медиаторов. Одновременно наблюдается низкое периферическое сосудистое сопротивление в результате системного раскрытия артериовенозных шунтов, которые активно функционируют при бактериемии. На определенном этапе развития сепсиса у больных регистрируется гиперкинетический тип гемодинамики с высоким сердечным выбросом. В последующем, по мере генерализации воспалительного процесса, происходит резкое снижение насосной функции сердца, сердечный выброс становится низким, системный кровоток уже не может компенсироваться за счет выраженной тахикардии. Отражением этой ситуации является развитие выраженной сердечной недостаточности. Диагностика септического миокардита осуществляется на основании вышеизложенных критериев диагностики миокардита и, конечно, учитывается наличие у больного сепсиса. Согласно решению Чикагской международной согласительной конференции (1991), сепсисом принято называть состояние, при котором наблюдается не менее двух признаков синдрома системного воспалительного ответа при наличии инфекционного очага (выявляемого клинически или подтвержденного бактериологически, но не обязательно с наличием бактериемии). Синдром системного воспалительного ответа - неспецифическая генерализованная реакция на инфекционный процесс. Синдром системного воспалительного ответа констатируется при наличии двух или более следующих клинических симптомов: температура тела выше 380С или ниже 36°С; частота сердечных сокращений выше 90; частота дыхания выше 20 или рСО2 ниже 32 мм рт. ст. (для больных на ИВЛ); количество лейкоцитов в периферической крови выше 12 х 109/л или ниже 4 х 109/л или незрелые формы лейкоцитов > 10%. Миокардит при инфекционном эндокардите Инфекционный эндокардит часто сопровождается развитием миокардита. Патологоанатомические и клинические проявления миокардита при инфекционном эндокардите те же, что при септическом миокардите, подробнее смотри в главе «Инфекционный эндокардит». Дифтерийный миокардит Дифтерия осложняется миокардитом в 6-8% случаев, а при тяжелом течении заболевания миокардит наблюдается почти у половины больных. Главным патогенетическим фактором дифтерийного миокардита является чрезвычайно высокая кардиотоксичность дифтерийного токсина и включение в патологический процесс аутоиммунного механизма, так как дифтерийный токсин вызывает выраженный распад кардиомиоцитов, компоненты которых становятся аутоан-тигенами. Кроме того, дифтерийный токсин сам является антигеном, причем существует определенное сходство антигена дифтерийного токсина с цитохромом ферментных систем кардиомиоцитов. Поэтому антитела к дифтерийному токсину блокируют цитохром кардиомиоцитов дополнительно к непосредственному ингибирующему влиянию токсина. В результате указанных процессов резко нарушается тканевое дыхание миокарда и образование в нем энергии и белка. Патоморфологические изменения при дифтерийном миокардите очень выражены. При макроскопическом исследовании обращают на себя внимание серовато-желтый цвет миокарда, его дряблость, дилатация полостей сердца. При микроскопическом исследовании отмечаются распад кардиомиоцитов, жировая инфильтрация, резкое поражение сосудов микроциркуляторного русла (деструкция сосудистой стенки, гиперемия сосудов, повреждение эндотелия), множественные геморрагии в периваскулярной и межмышечной строме. В межмышечной ткани выражен отек, выявляются клеточные инфильтраты, состоящие из гистиоцитов, лимфоцитов, плазмобластов, плазмоцидов, реже обнаруживаются нейтрофильные лейкоциты и эозинофилы. Наиболее пораженными оказываются стенки левого желудочка и папиллярные мышцы. Миокардит развивается обычно на 6-10 день от начала дифтерии, клиническая картина миокардита достигает максимальной выраженности к концу 2-3 недели, однако при молниеносной форме дифтерийный миокардит развивается чрезвычайно быстро и может в течение нескольких дней привести к смерти. Обычно миокардит развивается при средней степени тяжести и тяжелой дифтерии. Характеризуя клиническое течение миокардита при дифтерии. Он всегда протекает тяжело, клиническая симптоматика его выражена, на первый план выступают признаки СН, синоаурикулярная и атриовентрикулярная блокады, нарушения внутрижелудочковой проводимости, синдром слабости синусового узла, экстрасистолическая аритмия, пароксизмальная тахикардия. Более благоприятно протекает миокардит, который развивается на 3-4 неделе от начала заболевания. В отдельных случаях дифтерийный миокардит протекает в течение нескольких недель и месяцев. Миокардит при брюшном тифе Поражение миокарда при брюшном тифе чаще характеризуется миокардиодистрофией, реже - миокардитом. Морфологический вариант миокардита, наиболее часто развивающийся при брюшном тифе - это интерстициальный, реже - гранулематозный миокардит. В развитии интерстициального миокардита принимают участие преимущественно лимфоциты и гистиоциты, наблюдается пролиферация и слущивание эндотелия сосудов микpоциркуляторного русла, отек интерстициальной ткани. Гранулематозный миокардит характеризуется глыбчатым распадом коллагеновых волокон и формированием вокруг очагов распада тифоидных узелков (гранулом) - очагов фибрина и скопления эпителиоидных клеток. Миокардит развивается на 2-4-й неделе от начала заболевания, обычно при тяжелом его течении и при недостаточно эффективном лечении. Клиническая картина миокардита при брюшном тифе типичная, при этом редко наблюдаются мерцательная аритмия, полная атриовентрикулярная блокада, прогноз обычно благоприятный. Следует помнить о возможности развития послебрюшнотифозного миокардита через 1-2 недели после брюшного тифа. Туберкулезный миокардит Для туберкулеза наиболее характерно развитие хронического перикардита, миокардит развивается редко. Патоморфологические проявления миокардита зависят от формы туберкулеза. При первичном туберкулезе в миокарде обычно развивается узелковая, реже - диффузная макрофагальная реакция, формируются макрофагально-лимфоцитарные околососудистые гранулемы. При гематогенном туберкулезе в строме миокарда образуются туберкулезные бугорки, не содержащие сосудов, но имеющие участки творожистого некроза. При вторичном туберкулезе развивается интерстициальный миокардит. Клиническая картина туберкулезного миокардита характеризуется типичной симптоматикой, однако отличительной особенностью является значительное расширение не только левых, но и правых отделов сердца. Кроме того, туберкулезному миокардиту свойственно длительное и даже хроническое течение. Миокардит при клостридиальной инфекции При клостридиальной инфекции может наблюдаться множественное поражение органов, часто развивается миокардит. Поражение миокарда является следствием влияния на него клостридиального токсина. Типичным является обнаружение пузырьков газа в миокарде при патологоанатомическом исследовании, а также выраженных деструктивных изменений в миокардиальных волокнах, вместе с тем воспалительная инфильтрация обычно отсутствует. Clostridium perfringens может также вызвать формирование абсцессов в миокарде, перфорацию миокардиальной стенки и гнойный перикардит. Течение миокардита при клостридиальной инфекции тяжелое, прогноз неблагоприятен. Миокардит при легионеллезе Известно, что при легионеллезной инфекции (болезни легионеров) поражаются не только легкие, но и скелетная мускулатура (может отмечаться рабдомиолиз), почки (может развиться почечная недостаточность), печень, центральная нервная система, но поражение сердца считается не характерным или маловыраженным, проявляющимся только неспецифическими изменениями зубца Т, интервала ST. Однако иногда у больных развивается миокардит, в редких случаях с очагами некроза в миокарде, с застойной сердечной недостаточностью, возможно появление перикардиального выпота. Миокардит при менингококковой инфекции Миокардит может наблюдаться при менингококковой инфекции, но обычно при тяжелом течении менингита. Патоморфологические изменения в миокарде характеризуются воспалительными инфильтратами в интерстиции, состоящими из лимфоцитов, полиморфно-ядерных лейкоцитов, плазматических клеток, могут определяться миокардиальные некрозы. Менингококковый миокардит протекает типично, может приводить к развитию сердечной недостаточности. Возможно тяжелое течение миокардита с присоединением экссудативного перикардита и даже тампонады сердца. Менингококковый миокардит характеризуется также поражением проводящей системы сердца, атриовентрикулярного и синусового узлов, что может привести к внезапной смерти. Миокардит при микоплазменной пневмонии Клинически выраженный миокардит при пневмонии, вызванной микоплазмой, бывает редко. Чаще это миокардит, не проявляющийся клинически, но характеризующийся неспецифическими электрокардиографическими изменениями со стороны зубца Т и интервала ST, в редких случаях возможно развитие атриовентрикулярной блокады. Обычно электрокардиографические изменения исчезают через 1-2 недели. Причиной этих изменений считается аутоиммунный воспалительный процесс в миокарде. Однако возможно и тяжелое течение миокардита с развитием застойной сердечной недостаточности и присоединением экссудативного перикардита. У большинства больных наступает выздоровление, у некоторых пациентов возможно длительное течение миокардита с развитием сердечных аритмий. Миокардит при пситтакозе Миокардит при пситтакозе, вызванном Chlamydia psittaci, наблюдается довольно часто и характеризуется застойной сердечной недостаточностью и острым перикардитом. Возможно вовлечение в патологический процесс эндокарда, в этом случае развивается панкардит. Клиническая симптоматика поражения сердца включает лихорадку, кардиомегалию, застойную СН, артериальную гипотензию, ритм галопа, системные тромбоэмболии. Однако надо отметить, что лечение пситтакоза препаратами тетрациклинового ряда оказывается успешным и благоприятно влияет на течение миокардита. Миокардит при сальмонеллезе Клинически выраженный миокардит при сальмонеллезе наблюдается редко, обычно при тяжелом течении заболевания, преимущественно у детей, и ассоциируется с высокой смертностью. При тяжелой сальмонеллезной инфекции могут формироваться абсцессы в миокарде, которые могут разрываться и приводить к фатальной тампонаде сердца. Течение клинически выраженного миокардита обычно тяжелое, но развивается он постепенно, приводя к выраженной застойной сердечной недостаточности и тромбоэмболиям в сосуды большого и малого круга кровообращения. Все же у большинства больных миокардит протекает субклинически и проявляется преимущественно лишь неспецифическими изменениями зубца Т и интервала ST на электрокардиограмме. Миокардит при болезни Уиппла Болезнь Уиппла или кишечная липодистрофия - системное инфекционное заболевание тонкой кишки, вызываемое возбудителем Tropheryma whippelii, характеризующееся блокадой лимфатических сосудов тонкого кишечника, развитием синдрома экссудативной энтеропатии и нередко поражением других органов и систем. Заболевание развивается преимущественно у лиц со стойким угнетением Т-клеточного иммунитета. Возбудитель заболевания Tropheryma whippelii относится к некультивируемым грамотрицательным актиномицетам. Они обнаруживаются при электронной микроскопии внутри и вокруг макрофагов собственной пластинки слизистой оболочки тонкой кишки, в энтероцитах и макрофагах, в виде палочковидных образований размерами 0,3 х (1,5-2,5) мкм. В основе заболевания лежит закупорка лимфатических сосудов тонкого кишечника PAS-положительными макрофагами. Основными симптомами заболевания являются боли в животе неопределенного характера, поносы, стеаторея, значительное снижение массы тела, синдром нарушенного всасывания, субфебрильная температура тела, полиартралгии, лимфаденопатия (увеличение забрюшинных и реже периферических лимфоузлов), полисерозит. Возможно появление геморрагии и узловатой эритемы на коже. У некоторых больных наблюдаются симптомы поражения нервной системы с парезом глазодвигательных мышц, атаксией, тремором. Поражение миокарда наблюдается у 1/3 больных с болезнью Уиппла. В миокарде, а также в перикарде, створках клапанов обнаруживаются PAS-положительные макрофаги. Наблюдаются повреждения коронарных артерий с некрозами их гладкой мускулатуры. В миокарде могут обнаруживаться воспалительные инфильтраты и даже рубцовые изменения. Клинически миокардит при болезни Уиппла проявляется кардиомегалией, застойной сердечной недостаточностью, развитием аритмий сердца. В связи с фиброзом клапана аорты и митрального клапана появляется звуковая симптоматика их недостаточности. Основным методом диагностики болезни Уиппла является гистологическое исследование биоптатов слизистой оболочки тонкой кишки, полученных во время фибродуоденоскопии. В биоптатах определяется инфильтрация собственной пластинки слизистой оболочки тонкой кишки крупными, пенистыми PAS-положительными макрофагами. Они обнаруживаются также в лимфатических узлах, биоптатах миокарда, печени, нервных стволов. Миокардит при лептоспирозе Васильева-Вейля При лептоспирозе Васильева-Вейля поражение миокарда чаще всего протекает субклинически, однако если при тяжелом течении лептоспироза развивается миокардит, то обычно он характеризуется очень выраженной симптоматикой и тяжелым течением. Выраженный миокардит при лептоспирозе характеризуется появлением мерцательной аритмии, атриовентрикулярной блокады I-II степени, возможно развитие сердечной недостаточности, перикардита. На электрокардиограмме обнаруживаются неспецифические изменения интервала ST и зубца Т. При патологоанатомическом исследовании сердца больных, погибших при фатальном течении лептоспироза, обнаруживаются обширные геморрагические инфильтраты в межуточной ткани миокарда, аорты, коронариит. Миокардит при болезни Лайма Болезнь Лайма - системный клещевой боррелиоз, природноочаговая трансмиссивная инфекционная болезнь, вызываемая Borrelia burgdorferi, и протекающая с распространенной кожной эритемой, лихорадкой, признаками поражения центральной и периферической нервной системы, сердца и крупных суставов. Название заболевания происходит от города Лайм в штате Коннектикут (США), в котором в 1982 г. Burgdorfer выделил из иксодова клеща возбудителя болезни, относящегося к спирохетам. Резервуаром обитания боррелий являются мелкие и крупные дикие (грызуны, сумчатые, олени, птицы) и некоторые домашние (кошки, собаки, овцы, крупный рогатый скот) животные, выделяющие возбудителя с мочой. Переносчиком инфекции являются иксодовые клещи. Механизм заражения - трансмиссивный, через укус клеща. Распространенность заболевания совпадает с ареалом иксодовых клещей - северо-восточные и центральные регионы США, Китай, Япония, Австралия, Западная Сибирь, Дальний Восток. В месте укуса клеща возбудитель болезни проникает в кожу, вызывая развитие хронической мигрирующей эритемы, а также проникает в кровь и вместе с кровью распространяется по всему организму. Инкубационный период составляет от 3 до 32 дней. Заболевание протекает в три фазы. I фаза - общетоксическая длится от 3 до 35 дней, проявляется лихорадкой, головными болями, миалгиями, полиартралгиями, тошнотой, симптомами фарингита, увеличением периферических лимфоузлов, печени, селезенки. В месте укуса клеща появляется папула, затем кольцевидная эритема, в последующем у 75% больных принимающая длительное, хроническое мигрирующее течение. II фаза - диссеминированная инфекция - развивается на 4-5 неделе и продолжается в течение 1-2 месяцев. В этой фазе наступает гематогенная диссеминация возбудителя. Наиболее существенными проявлениями болезни являются неврологические и кардиальные нарушения. Поражение нервной системы характеризуется симптомами серозного менингита, менингоэнцефалита, энцефаломиелита с пара- и тетрапарезами, парезами лицевого нерва, глазодвигательного нерва, часто развивается полирадикулоневрит. Поражение сердца наблюдается у 8-10% больных. Характерно развитие атриовентрикулярной блокады различных степеней, при этом нередко возникает полная блокада с развитием синкопальных состояний. Возможна симптоматика типичного диффузного миокардита с кардиомегалией и сердечной недостаточностью, но все-таки это бывает редко. У некоторых больных развивается миоперикардит. Симптомы поражения сердца сохраняются около 6 недель, в дальнейшем у большинства больных наступает нормализация функций сердца. У отдельных больных в биоптатах миокарда обнаруживаются боррелий, что является прямым диагностическим признаком заболевания и подтверждает точку зрения о том, что повреждение сердца обусловлено непосредственным внедрением возбудителя в миокард и воздействием его токсинов. Для диагностики повреждения миокарда при болезни Лайма применяют ЭКГ (выявляются нарушения атриовентрикулярной проводимости, неспецифические изменения зубца Т и интервала ST), радиоизотопное сканирование миокарда с радиоактивным галлием (накапливается в очагах поражения миокарда) или сканирование с применением антимиозиновых антител, меченных радиоактивным индием (антитела концентрируются в пораженных участках миокарда). III фаза (артритическая) развивается через 6 и более недель от начала болезни (иногда через 2-3 месяца) и характеризуется поражением суставов в виде асимметричных артритов коленных и локтевых, межфаланговых, височно-челюстных суставов. Пораженные суставы болезненны, отечны, однако почти не гиперемированы. Возможны неоднократные рецидивы полиартрита, которые могут длиться несколько недель и даже месяцев. Однако развитие хронического артрита или полиартрита с развитием эрозий суставных поверхностей костей с разрушением хряща наблюдается лишь у отдельных больных. III фаза называется многими исследователями также хронической (Steere, 1998), потому что в этой стадии проявляется хроническое поражение нервной системы (энцефалопатия, полинейропатия, энцефаломиелит), кожи (хронический атрофический акродер-матит) и возможен рецидивирующий полиартрит. Диагноз болезни Лайма ставится на основании следующих признаков: укусы клеща в анамнезе; появление мигрирующей кольцевидной эритемы с последующими признаками поражения нервной системы, сердца, суставов,обнаружение боррелий в спинномозговой жидкости, синовиальной жидкости, биоптатах кожи; определение наличия и концентрации специфических антителк боррелиям в организме больного такими методами, как им-мунофлюоресценция, реакция связывания комплемента, реакция непрямой гемагглютинации, иммуноферментный анализ ииммунный блоттинг. Наиболее точными методами являютсяиммуноферментный анализ и иммуноблоттинг. Антитела к боррелиям обычно появляются у больных с болезнью Лайма на 3-6 неделе от начала заболевания, причем вначале образуются антитела класса Ig M, в более поздние сроки (через 1 месяц и позже) - антитела класса Ig G; определение ДНК боррелий методом полимеразной цепной реакции в биологическом материале: в кожном биоптате, крови, моче, суставной и цереброспинальной жидкости. Метод высокочувствителен и позволяет определить инфицированность пациента на 7 день от момента присасывания клеща, часто еще в инкубационном периоде. Грибковые поражения миокарда Грибковые поражения сердца являются довольно редкой патологией и наблюдаются лишь при тяжелом генерализованном течении грибковой инфекции. Обычно это бывает у больных, получавших массивную, длительную антибиотикотерапию, а также длительно и в больших дозах принимавших глюкокортикоидные препараты. Кроме того, генерализованная грибковая инфекция налюдается у больных СПИДом. Наиболее частыми видами грибковой инфекции, встречающимися в практике врача, являются актиномикоз, аспергиллез, кандидамикоз. При генерализованном течении чаще возникают перикардит и эндокардит. Миокард вовлекается в патологический процесс редко. При генерализованном актиномикозе актиномицеты могут проникать в миокард, вызывать развитие некротизирующих абсцессов, окруженных грануляционной тканью. При этом отмечается тяжелая сердечная недостаточность. Поражение перикарда при актиномикозе характеризуется появлением выпота в полости перикарда, в последующем развитием констриктивного перикардита. Поражение миокарда при аспергиллезе наблюдается редко, но если оно возникает, то может привести к летальному исходу. При патологоанатомическом исследовании больных, погибших от генерализованного аспергиллеза, в миокарде обнаруживаются грибковые мицеллы, абсцессы и некрозы миокарда. Кандидамикозное поражение миокарда обнаруживается также только при генерализованном течении кандидамикоза, в миокарде возможно развитие абсцессов, причем микроабсцессы локализуются чаще всего в области АВ-соединения и межжелудочковой перегородки, что приводит к развитию атриовентрикулярной блокады. О грибковом поражении миокарда можно думать у больных с тяжелым, генерализованным системным микозом (обычно у лиц с выраженным иммунодефицитом, длительно лечившихся глюкокортикоидами, антибиотиками, цитостатиками) при наличии электрокардиографических изменений и клинических признаков дисфункции миокарда. У большинства больных при этом определяются симптомы поражения перикарда, а также почек, легких и других органов. Миокардит при трипаносомозе Трипаносомоз (болезнь Чагаса) - заболевание, вызываемое разновидностью простейших Tripanosoma cruzi (описана впервые Chagas в 1909 г.). Заболевание распространено преимущественно в Центральной и Южной Америке, Бразилии, Аргентине, Чили. В этих странах болезнь является ведущей причиной смерти в группе сердечно-сосудистых болезней. В настоящее время Tripanosoma cruzi инфицированы около 20 млн. человек. На других континентах, кроме Америки, заболевание не встречается. Tripanosoma cruzi передается от млекопитающего к млекопитающему триатомовыми клопами, которые заражаются при заглатывании крови инфицированного животного или человека. В кишечнике клопа трипаносомы подвергаются ряду превращений, размножаются и выделяются с экскрементами клопа во время последующего кровососания Заражение человека происходит при попадании экскрементов клопа на участки поврежденной кожи и слизистые оболочки (например, конъюнктивы). Кроме того, возможно заражение от инфицированного человека при переливании его крови, при контакте с его кровью, а также трансплацентарным путем. Первые симптомы болезни появляются приблизительно через 7-10 дней после заражения. Различают 3 фазы болезни: острую, латентную и хроническую. В острой фазе болезни в месте внедрения возбудителя появляется припухлость и покраснение кожи, увеличиваются регионарные лимфоузлы, при внедрении инфекции через конъюнктиву появляется отек век и периорбитальных тканей (симптом Романьи). Кроме местных проявлений наблюдаются общая слабость, лихорадка, отсутствие аппетита, отеки нижних конечностей, лица, увеличение печени, селезенки, периферических лимфоузлов. В острой фазе болезни Чагаса возможно развитие миокардита. Трипаносомы проникают в миокард, вызывают развитие воспалительной клеточной инфильтрации, деструкцию кардиомиоцитов. В развитии миокардита при болезни Чагаса большое значение придается также развитию аутоиммунных процессов в миокарде и повреждающему влиянию цитотоксических Т-лимфоцитов. Миокардит в острой фазе заболевания имеет типичную клиническую картину и протекает обычно тяжело. В острой фазе возможно также развитие экссудативного перикардита, эндокардита, образование внутрисердечных тромбов. Однако постепенно все проявления острой фазы стихают, и больные вступают в латентную фазу заболевания. В этой фазе болезни нет отчетливой клинической симптоматики, однако в это время формируется кардиомиопатия, проявляющаяся неспецифическими изменениями электрокардиограммы. Хроническая фаза болезни Чагаса развивается спустя годы после заражения и наблюдается у 30% больных. Важнейшей особенностью хронической фазы является поражение сердца в виде синдрома дилатационной кардиомиопатии и недостаточности кровообращения. Основными клиническими симптомами являются слабость, головокружения, одышка, отечность голеней и стоп, тахикардия, расширение границ сердца влево, глухость тонов сердца, часто протодиастоличес-кий ри Смотрите также: Боковой амиотрофический склероз, Гипертрофическая кирдиомиопатия, Миома матки при беременности, Гликогеноз VII типа (болезнь Таруи, миофосфофруктокиназная недостаточность), Спинальная амиотрофия Верднига–Гоффманна, Миоклоническая эпилепсия раннего детского возраста, Подслизистая (субмукозная) миома матки, Миокардит у детей, Миома матки, Миокардиодистрофия у детей |